Microbiota intestinal e o sistema imune
A imunidade intestinal exerce papel central na manutenção da saúde dos suínos. Em animais gnotobióticos, o sistema imune intestinal é subdesenvolvido, com deficiência na produção de muco, peptídeos antimicrobianos e na presença de componentes como anticorpos e células T (Gewirtz et al., 2001). A presença da microbiota associada à mucosa intestinal é determinante para a modulação e maturação imunológica (Mulder et al., 2011; Arpaia et al., 2013; Belkaid & Hand, 2014), uma vez que a maioria dos genes que influenciam o microbioma está relacionada ao sistema imune. Os elementos imunológicos do hospedeiro exercem uma seleção ativa sobre os microrganismos do lúmen intestinal, moldando uma microbiota benéfica (Honda; Littman, 2016).
Além disso, microrganismos comensais podem:

- metabolizar toxinas alimentares
- sintetizar vitaminas
- promover a maturação das células epiteliais intestinais
- e reforçar a função de barreira, favorecendo a homeostase imunológica.
(Kabat; Srinivasan; Maloy, 2014; Yang et al., 2016; Li et al., 2018; De Vries; Smidt, 2020).
Mecanismos de tolerância e resposta ao microbioma intestinal
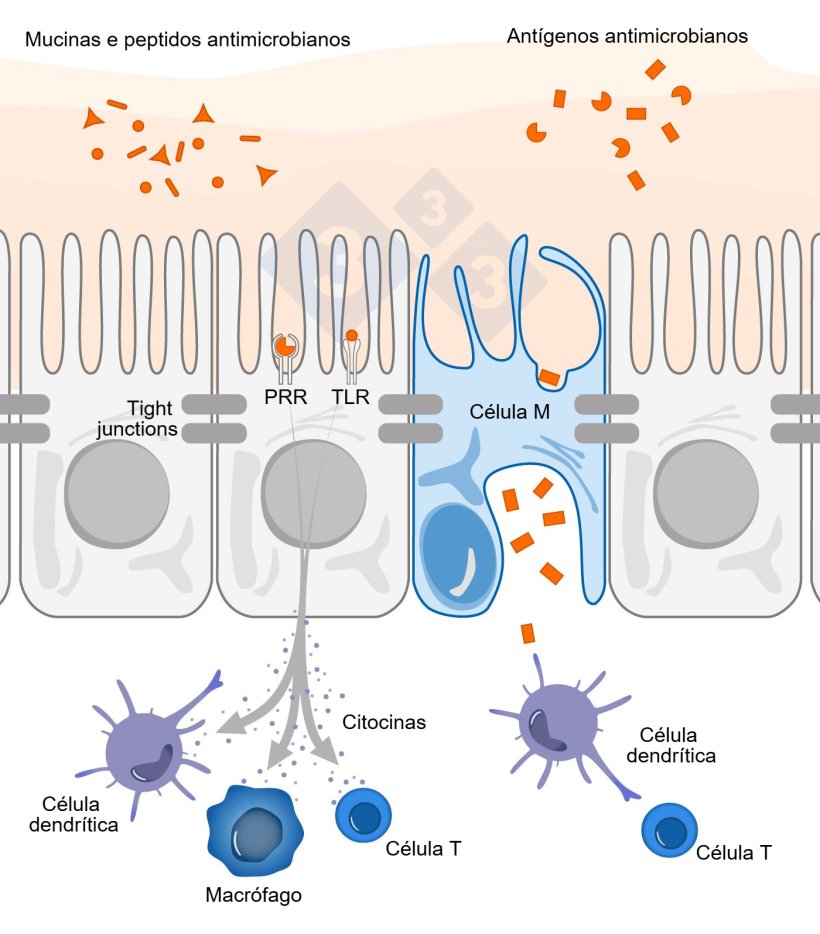
A crescente valorização da microbiota intestinal como fator determinante no desempenho dos suínos motivou avanços no estudo de seus mecanismos de interação com a imunidade (Duarte; Kim, 2022). A modulação do microbioma impacta diretamente o desenvolvimento da imunidade e das funções intestinais (Chen et al., 2018; Li et al., 2018). A densidade bacteriana aumenta ao longo do trato gastrointestinal, e o sistema imune precisa distinguir microrganismos patogênicos de comensais ou inofensivos (Stokes, 2017). Essa tolerância seletiva é essencial para evitar reações inflamatórias desnecessárias, preservando a integridade mucosa (Brown; Sadarangani; Finlay, 2013; Mowat, 2018). Por estas razões, o sistema imune intestinal utiliza de diferentes mecanismos frente ao microbioma para assegurar sua homeostase (Figura 1):
As tight junctions são estruturas fundamentais na restrição da permeabilidade transepitelial. Sinais derivados dos microrganismos fortalecem essa barreira ao induzir a regulação positiva de seus componentes entre os enterócitos e a modificação de proteínas do citoesqueleto (Bansal et al., 2010).
Os peptídeos antimicrobianos (AMPs) também interagem com a microbiota, contribuindo para sua modulação e promovendo a eliminação de bactérias comensais próximas ao epitélio (Macpherson; Uhr, 2004; Hooper; Littman; Macpherson, 2012).
A expressão de receptores de reconhecimento de padrão (PRRs) é essencial para a homeostase intestinal. Eles detectam os MAMPs (padrões moleculares associados a microrganismos) e regulam a produção de mucina, AMPs, IgA, citocinas, além da manutenção das tight junctions e proliferação epitelial. Esses ligantes não são exclusivos de patógenos e são amplamente produzidos pela microbiota comensal durante a colonização saudável (Brown; Sadarangani; Finlay, 2013; Chu; Mazmanian, 2013).
Os receptores tipo Toll (TLRs), reconhecem padrões moleculares conservados compartilhados por grandes grupos de bactérias e outros microrganismos intestinais (Shi et al., 2017). Estudos sugeriram que os TLRs são estrategicamente expressos na região basolateral das células epiteliais intestinais, para que não sejam expostos à microbiota no lúmen. Entretanto, novas descobertas revelaram que os TLRs também estão expressos apicalmente. Assim, mesmo se ocorrer uma falha no reconhecimento destes microrganismos, as células da imunidade inata estarão prontas para atuar (Kayisoglu et al., 2020; Schären; Hapfelmeier, 2021).
Os macrófagos intestinais também exercem papel essencial na tolerância à microbiota comensal. Eles expressam um fenótipo hipo-responsivo aos ligantes de TLRs, com baixa expressão de moléculas coestimulatórias (CD40, CD80, CD86) e elevada produção de IL-10 (capacidade anti-inflamatória), além de reduzida síntese de citocinas pró-inflamatórias e óxido nítrico. Isso promove o equilíbrio entre linfócitos Th efetores e T reguladores, sustentando a homeostase (Lopes; Mosser; Gonçalves, 2020).
Apesar das barreiras inatas entre microbiota e epitélio, células dendríticas atuam ativamente na regulação imune. Elas projetam dendritos através da barreira intestinal para capturar microrganismos no lúmen (Brown; Sadarangani; Finlay, 2013; Shi et al., 2017), promovendo a produção de IgA secretora e regulando a resposta imune (Gonçalves et al., 2016; Zheng; Liwinski; Elina, 2020).
Microrganismos comensais eventualmente atravessam a camada de muco no intestino delgado (Ermund et al., 2013). Nesses casos, são apresentados aos linfócitos B e T pelas células dendríticas, induzindo a produção de IgA (Chen et al., 2021). Esses linfócitos também são submetidos a mecanismos de tolerância, uma vez que expressam receptores específicos para os antígenos microbianos (Bailey et al., 2005). Por fim, a relação entre IgA e microbiota é mutualística: um repertório diverso e bem regulado de IgA contribui para a manutenção de um microbioma equilibrado (Gutzeit; Magri; Cerutti, 2014; Kawamoto et al., 2014).
Conclusão
A imunidade intestinal é um sistema complexo, composto por barreiras físicas, células imunes, receptores e microbiota. Em equilíbrio, protege contra patógenos e favorece o desempenho dos suínos. Entretanto, fatores como estresse, desmame precoce e infecções podem comprometer essa defesa, levando a inflamações e prejuízos produtivos. Compreender a complexidade da imunidade intestinal e buscar estratégias para preservá-la é essencial para uma produção eficiente, rentável e sustentável.



